南京大学医学院杨中州教授团队发现胎盘发育异常与胚胎心脏发育缺陷之间的联系
来源:南京大学医学院 时间:2025-03-07 05:36:27
先天性心脏病是常见的出生缺陷。遗传因素和环境因素在先天性心脏病的发生过程中起到重要的作用。目前已知少于50%的心脏发育缺陷与遗传因素相关,提示环境因素在其发生过程中的作用不容小觑。胎盘作为母亲与胎儿之间的交互界面,为胚胎发育提供营养物质和氧气,并将胚胎的代谢废物转运至母体。二十年多前,人们在小鼠遗传学的研究中发现胎盘发育不良会导致心脏发育缺陷,提出了“胎盘-心脏发育调控轴”的概念,但其中的调控关系与机制尚不明了。
南京大学医学院杨中州教授团队多年来一直利用小鼠模型研究心脏发育的调控机制以及心脏发育缺陷发生的机理,帮助理解先天性心脏病的发生原因。为此,他们围绕22q11.2缺失综合征(DiGeorge综合征)开展工作,该综合征的患者中大部分都表现出心脏发育异常。 在22q11.2缺失片段中有大约50个编码基因,除了Tbx1在心脏发育中的作用比较清楚之外,对其它基因与心脏发育的关系所知甚少。在上述约50个编码基因当中,有9个与线粒体功能有关,提示线粒体功能可能在心脏发育中发挥重要的作用,其中一个基因是Slc25a1,编码柠檬酸转运体SLC25A1,可以将线粒体中的柠檬酸转运至细胞质中。
为了研究Slc25a1在心脏发育中的作用,他们培育出了全身敲除Slc25a1的小鼠,发现心脏发育出现异常及神经管闭合不全。于是,他们利用几个心脏特异表达Cre小鼠,在心脏组织中特异敲除Slc25a1。令人惊讶的是,这些小鼠并未出现心脏缺陷,表明 SLC25A1 在心脏组织细胞中并未发挥重要作用,提示胎盘发育异常可能是导致胚胎心脏发育缺陷发生的原因。接下来,他们培育出仅在胎盘组织中缺失 SLC25A1 蛋白的小鼠,他们发现这些小鼠既出现了胎盘缺陷,也出现了心脏发育缺陷。这表明 SLC25A1 在胎盘发育过程中起着关键作用,并进而指导胚胎心脏发育。通过单细胞 RNA 测序分析发现,Slc25a1的缺失影响胎盘滋养层细胞分化,尤其是海绵滋养层(SpT)和糖原滋养层(Gly-T)细胞,以及迷路滋养层祖细胞向合胞体滋养层(SynT)-I 和 SynT-II 细胞的分化。机制研究发现,SLC25A1 通过调节组蛋白 H3K27 乙酰化(H3K27ac)水平,影响调控滋养层发育关键基因启动子和增强子区域的 H3K27ac 占位,进而影响到这些基因的表达,指导滋养层细胞分化与胎盘发育,保证胚胎心脏的正常发育。此外,他们还发现妊娠特异性糖蛋白 1(PSG1)在 SLC25A1缺失胎盘中表达下调,给孕鼠补充人重组 PSG1 蛋白可部分挽救 SLC25A1缺失小鼠的胎盘和心脏发育表型。
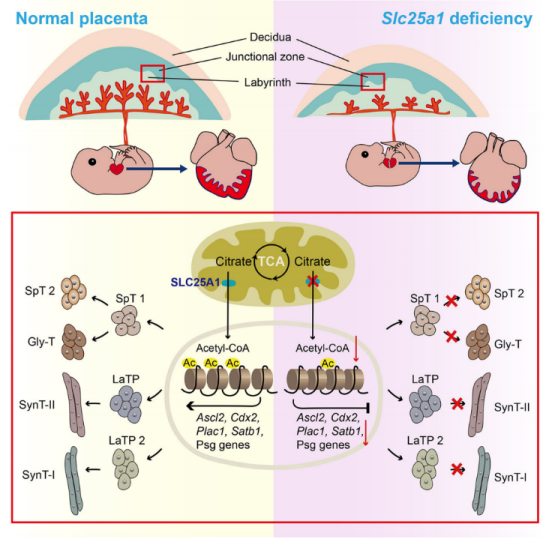
上述研究结果于近期发表于发育生物学领域重要期刊Development杂志,题目为“SLC25A1 regulates placental development to ensure embryonic heart morphogenesis”。该研究首次利用胎盘特异性敲除小鼠证明了胎盘形成相关基因对胚胎心脏发育的影响,加深了对“胎盘 - 心脏发育轴”的理解,为治疗胚胎心脏发育缺陷提供了新思路。该研究被选为Research Highlight,并配发了“文章背后的人物(The people behind the papers)”访谈。另外,编辑还撰写了新闻报道(Press release), 在美国科学促进会(AAAS)新闻网站EurekAlert对该研究进行了宣传,被多个网站广泛引用和转发。

南京大学博士研究生范文丽为本文第一作者。南京大学杨中州教授、南京大学医学院宿迁研究院孙明主任为共同通讯作者。该项研究得到了国家自然科学基金委与科技部重点研发专项以及基因组资源国际联合研究中心项目的基金支持,厦门大学王海滨教授为该研究提供了胎盘特异Cre小鼠。
原文链接:https://doi.org/10.1242/dev.204290







